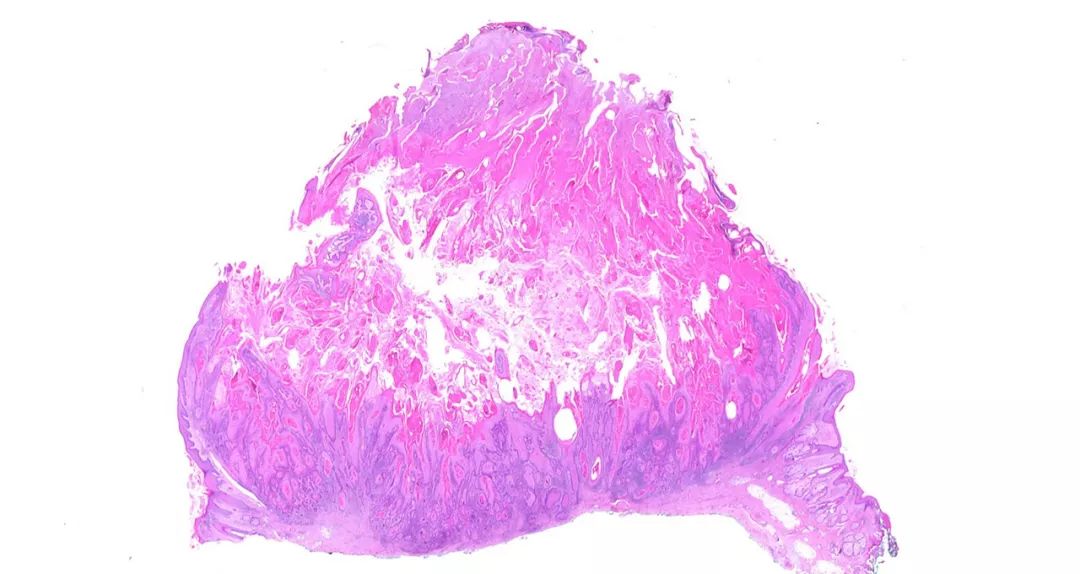
显微镜下:顶尖病理实验室融合数据源,研发癌症检测AI应用
2019-11-11 21:40
近期一项研究表明,病理学家在基于活检标本进行乳腺癌诊断时,仅四分之三的情况下能够达成一致诊断。
组织切片的分析过程难度高且耗时,这就是为什么病理学在各个医院中都是费用最昂贵的项目之一。
哈佛医学院(Harvard Medical School)和布莱根妇女医院(Brigham and Women’s Hospital)的病理学助理教授Faisal Mahmood带领团队开发了一种深度学习工具,可将来自数字化整体切片病理学数据、分子信息和基因组学等多重来源的信息相结合,助力病理学家提高癌症诊断的准确性。
Mahmood在布莱根妇女医院的计算病理学部门带领着以其命名的Mahmood实验室(Mahmood Lab),他于上周举行的GTC DC(GPU技术大会华盛顿场)上谈到了这项研究。
他在近期一次采访中说道,病理学家诊断上的变数“可能会带来可怕的后果,因为不确定的判断可能会导致多余的活检和不必要的干预性手术。深度学习在诊断和治疗反应预测方面颇具潜力,能够减少主观性偏见。”
根据癌症类型和病理学家的经验,病理学家对活检切片的分析可能需要15分钟或更长时间。如果一个病人有几十张切片,分析诊断所需的时间就会大幅增加。
在制定治疗方案时,医生也会将其他数据来源纳入考量,如患者及家族病史,以及可用的分子和基因组数据。
Mahmood的团队使用本地和云端的NVIDIA GPU开发了用于病理图像分析的AI工具,将所有这些数据源整合到了一起。
Mahmood表示:“通过处理整张切片图像并融合多重模态数据源,我们的算法也日渐贴近临床工作流程。这将使我们能够借助使用多重模态数据的AI辅助病理诊断工具来进行前瞻性研究。”
AI识别大图
在组织活检整张切片的数字化图像很大——每张可能超过10万×10万像素。为对如此大的文件进行高效计算,深度学习开发者通常会选择将切片分割成单独的小块,从而更易于神经网络进行处理。但这种方式需要研究人员手工标记训练数据,非常耗时。
Mahmood实验室正在开发一种深度学习模型,使用NVIDIA GPU加速神经网络的训练和推理,以一种数据高效型的方式对整体组织切片进行一次性解析。这些模型可用于患者选择和治疗分组,以开展精确的治疗。
为制作深度学习模型原型并进行推理,该团队采用了四台搭载NVIDIA GPU集群的本地机器。为训练图卷积网络和具有大型病理图像的对比预测编码模型,研究人员在Google Cloud中使用了NVIDIA V100 Tensor Core GPU 。
Mahmood实验室研究员Max Lu说道:"现代GPU让我们能够在整张切片上训练深度学习模型。其优势就在于无需对当前临床工作流程做出调整,因为病理学家的分析和报告的准备都是针对整张切片。"
结合多源信息
病理学家的判断通常要基于大量数据,包括组织切片、免疫组织化学标记和基因组图谱,但目前大多数基于深度学习的诊断方法是依赖单一数据源或简单的信息融合。
为此,Mahmood实验室的研究人员开发出了一种机制,将显微镜和基因组数据以一种更具启发性和整体性的方式相结合。初步结果表明,添加来自基因组图谱和图卷积网络的信息能够完善诊断和预后模型。
融入病理工作流程
Mahmood认为有两种潜在方法能够将深度学习融入到病理学家的工作流程中。AI注释的切片图像可为病理学家提供辅助意见,以助力提高诊断的质量和一致性。
亦或,计算病理学工具可筛选出所有阴性病例,这样病理学家只需查看可能为阳性的活检切片,从而大幅减少病理学家的工作量。这种方式此前就有先例:上世纪90年代,医院开始使用第三方公司对巴氏涂片进行扫描和分层,剔除所有阴性病例。
Mahmood说道:“如果有4万张乳腺癌组织切片,其中2万张是阴性的,那么这一半就会被分层,病理学家就无需过目了。仅通过减轻病理学家的负担,诊断的差异性就会降低。”
为对算法进行测试和验证,研究人员计划使用来自丹娜法伯癌症研究院(Dana Farber Cancer Institute)的活检数据进行回顾性和前瞻性研究。他们将研究病理学家在看到算法的判断后,对活检切片的分析是否会发生变化,以及使用AI是否会降低诊断中的差异性。
组织切片的分析过程难度高且耗时,这就是为什么病理学在各个医院中都是费用最昂贵的项目之一。
哈佛医学院(Harvard Medical School)和布莱根妇女医院(Brigham and Women’s Hospital)的病理学助理教授Faisal Mahmood带领团队开发了一种深度学习工具,可将来自数字化整体切片病理学数据、分子信息和基因组学等多重来源的信息相结合,助力病理学家提高癌症诊断的准确性。
Mahmood在布莱根妇女医院的计算病理学部门带领着以其命名的Mahmood实验室(Mahmood Lab),他于上周举行的GTC DC(GPU技术大会华盛顿场)上谈到了这项研究。
他在近期一次采访中说道,病理学家诊断上的变数“可能会带来可怕的后果,因为不确定的判断可能会导致多余的活检和不必要的干预性手术。深度学习在诊断和治疗反应预测方面颇具潜力,能够减少主观性偏见。”
根据癌症类型和病理学家的经验,病理学家对活检切片的分析可能需要15分钟或更长时间。如果一个病人有几十张切片,分析诊断所需的时间就会大幅增加。
在制定治疗方案时,医生也会将其他数据来源纳入考量,如患者及家族病史,以及可用的分子和基因组数据。
Mahmood的团队使用本地和云端的NVIDIA GPU开发了用于病理图像分析的AI工具,将所有这些数据源整合到了一起。
Mahmood表示:“通过处理整张切片图像并融合多重模态数据源,我们的算法也日渐贴近临床工作流程。这将使我们能够借助使用多重模态数据的AI辅助病理诊断工具来进行前瞻性研究。”
AI识别大图
在组织活检整张切片的数字化图像很大——每张可能超过10万×10万像素。为对如此大的文件进行高效计算,深度学习开发者通常会选择将切片分割成单独的小块,从而更易于神经网络进行处理。但这种方式需要研究人员手工标记训练数据,非常耗时。
Mahmood实验室正在开发一种深度学习模型,使用NVIDIA GPU加速神经网络的训练和推理,以一种数据高效型的方式对整体组织切片进行一次性解析。这些模型可用于患者选择和治疗分组,以开展精确的治疗。
为制作深度学习模型原型并进行推理,该团队采用了四台搭载NVIDIA GPU集群的本地机器。为训练图卷积网络和具有大型病理图像的对比预测编码模型,研究人员在Google Cloud中使用了NVIDIA V100 Tensor Core GPU 。
Mahmood实验室研究员Max Lu说道:"现代GPU让我们能够在整张切片上训练深度学习模型。其优势就在于无需对当前临床工作流程做出调整,因为病理学家的分析和报告的准备都是针对整张切片。"
结合多源信息
病理学家的判断通常要基于大量数据,包括组织切片、免疫组织化学标记和基因组图谱,但目前大多数基于深度学习的诊断方法是依赖单一数据源或简单的信息融合。
为此,Mahmood实验室的研究人员开发出了一种机制,将显微镜和基因组数据以一种更具启发性和整体性的方式相结合。初步结果表明,添加来自基因组图谱和图卷积网络的信息能够完善诊断和预后模型。
融入病理工作流程
Mahmood认为有两种潜在方法能够将深度学习融入到病理学家的工作流程中。AI注释的切片图像可为病理学家提供辅助意见,以助力提高诊断的质量和一致性。
亦或,计算病理学工具可筛选出所有阴性病例,这样病理学家只需查看可能为阳性的活检切片,从而大幅减少病理学家的工作量。这种方式此前就有先例:上世纪90年代,医院开始使用第三方公司对巴氏涂片进行扫描和分层,剔除所有阴性病例。
Mahmood说道:“如果有4万张乳腺癌组织切片,其中2万张是阴性的,那么这一半就会被分层,病理学家就无需过目了。仅通过减轻病理学家的负担,诊断的差异性就会降低。”
为对算法进行测试和验证,研究人员计划使用来自丹娜法伯癌症研究院(Dana Farber Cancer Institute)的活检数据进行回顾性和前瞻性研究。他们将研究病理学家在看到算法的判断后,对活检切片的分析是否会发生变化,以及使用AI是否会降低诊断中的差异性。

 分享到微信
分享到微信
 分享到微博
分享到微博